Існують органічні сполуки, молекули яких містять невелику кількість атомів водню, хоча їх карбоновий скелет досить великий. Такі речовини вважаються сильно ненасиченими, однак, вони не вступають в реакції, характерні для алкенів або алкіной. Наприклад, не знебарвлюють розчини перманганату калію або бромної води. Першими, отриманими хіміками з цієї групи сполук, виявилися речовини, що володіють приємним запахом, тому їх назвали ароматичними. Існує ще одна назва – арени. Номенклатура, ізомерія, одержання і фізичні властивості їх будуть вивчені нами в цій статті.

Що таке бензол
Найпростішим представником аренів є бензол. Молекулярна формула речовини – C6H6. Серед інших ароматичних вуглеводнів він має найбільш важливе практичне значення. З’єднання було виявлено в 1825 році англійським фізиком М. Фарадеєм у складі світильного газу. Воно являє собою безбарвну рідину, легше води (щільність 0,88 г/см3). Має характерний запах, отруйна. Температура кипіння – 80, замерзає при 5,5. Фізичні властивості аренів, як і інших органічних речовин, залежать не тільки від якісного і кількісного складу, але і від будови їх молекул.
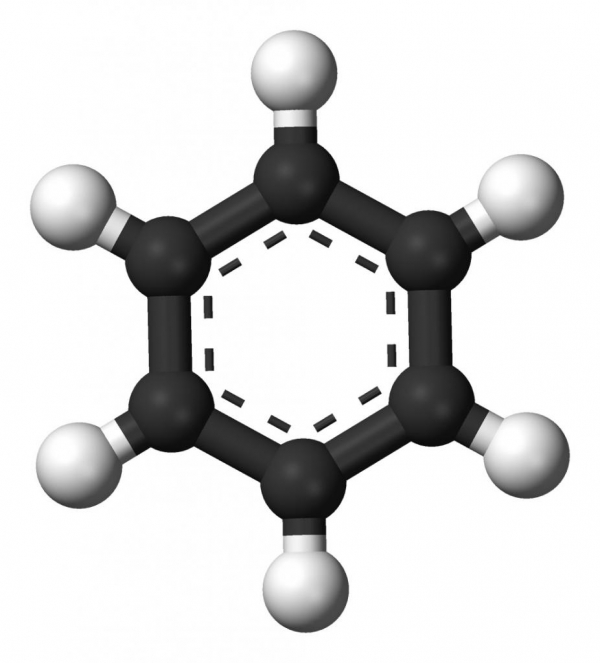
Загадка ароматичного ядра
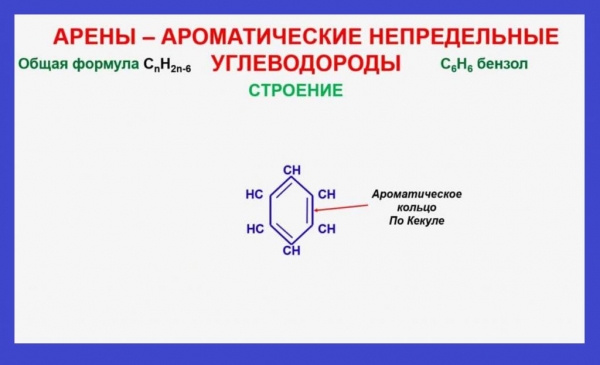
Перша структурна формула речовини була запропонована німецьким хіміком Кекуле. В ній атоми вуглецю лежать в одній площині і утворюють між собою правильний шестикутник. Частки карбону в молекулі з’єднані двома видами ковалентних зв’язків: одинарними і подвійними.Однак, експерименти не підтвердили наявність в бензолі пі-зв’язків, так як речовина не окислялось розчинами бромної води і перманганату калію. Поясненням цього протиріччя є електронна будова речовини. В його молекулі присутній особливий тип хімічного зв’язку, названий ароматичної або полуторною. Вона представлена загальним електронним хмара, що складається з шести взаємно перекриваються p-електронів. Розташовуючись над і під площиною молекули, зв’язок має вигляд кільця і називається ароматичним ядром. Полуторне зв’язок зумовлює фізичні властивості аренів, а також їх здатність до реакцій заміщення і приєднання.
Механізм процесу заміщення
Система ароматичного ядра має підвищену електронну щільність і може піддаватися атакам електрофільних частинок з дефіцитом негативних зарядів. Підсумком такого впливу буде заміщення атомів водню на інші частинки, наприклад, в молекулі бензолу. Фізичні властивості аренів та особливості перебігу хімічних процесів сильно відрізняються від таких у алканів або алкенів. Більш того, на відміну від інших класів органічних сполук, арени не можна описати однією загальною формулою. Так, для нафталіну формула буде мати наступний вигляд: c n h 2n-12, для бензолу –c n h 2n-6, для дифенила – c n h 2n-14.
Хлорування, бромирование і нітрування ароматичних вуглеводнів відбувається за єдиним механізмом електрофільного заміщення, у якому роль атакувального електрофільного агента грають аніони хлору, брому або нітрогрупи.
Чому реакції приєднання у аренів вимагають жорстких умов
Головна особливість будови молекул ароматичних сполук полягає у наявності в їх молекулах бензольного кільця, що складається з шести перекриваються між собою p-електронів. Від нього залежать основні хімічні характеристики та фізичні властивості аренів. Для розриву полуторним зв’язку необхідна додаткова значна порція енергії. Її отримують, застосовуючи наступні параметри: ультрафіолетове випромінювання, високу температуру і тиск в реагуючої суміші, а також використовуючи каталізатори. Наприклад, хлор приєднується до бензолу тільки при опроміненні ультрафіолетовим світлом, утворюючи гексахлорциклогексану (гексахлоран). Він застосовується для протравлення деревини в процесі її тривалого зберігання, а також у сільському господарстві як засоби для боротьби з комахами-шкідниками.

C6H6 + 3Cl2 —світло—> C6H6Cl6 – приєднання
Алкилбензолы
Якщо атоми водню в молекулі бензолу замістити вуглеводневими радикалами, наприклад, метильным -CH3 або этильным -C2H5, то отримані ароматичні вуглеводні не є простою сумою властивостей алканів і аренів. Фізичні властивості та хімічні реакції, характерні для цих сполук, будуть мати ряд відмінностей. Так, толуол та етилбензол є безбарвними рідинами зі своєрідним запахом, легші за воду і нерозчинні в ній. Зате речовини добре розчиняються в органічних розчинниках, наприклад, ацетоні або дихлорметане. Їх самих також можна застосовувати як розчинник. У ароматичних вуглеводнів існують і специфічні характеристики. Поверхневий натяг, коефіцієнт дифузії, в’язкість – це фізичні властивості аренів, коротко описують їх характеристику, як органічних розчинників.
Нітрування ароматичних сполук
Під дією азотної кислоти в присутності сульфатної кислоти як каталізатора арени піддаються нітруванні. Реакція бензолу з нітруючою сумішшю буде мати наступний вигляд.
Нітробензол являє собою маслянисту рідина блідо–жовтого кольору, має характерний запах мигдалю. Він застосовується як розчинник і служить вихідною сировиною для виробництва аніліну.
В реакції нітратної кислоти з толуолом утворюється вибухова речовина – тринітротолуол або тротил. Як пірогенних з’єднань застосовують і деякі інші органічні речовини з бензольными ядрами, що містять кратні зв’язки в бічних ланцюгах.
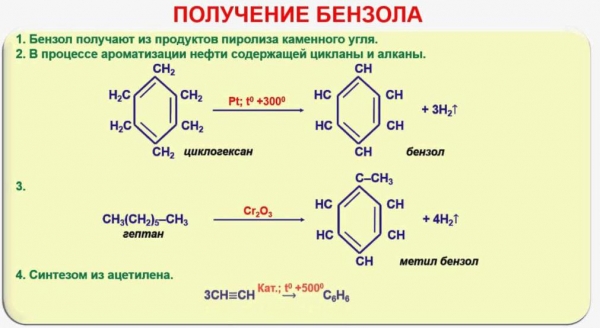
Отримання і застосування аренів
Фізичні властивості аренів: високу теплоємність, горючість, здатність розчиняти інші речовини, широко використовують у різних господарських галузях. Бензол, толуол, нафталін, антрацен та інші ароматичні вуглеводні одержують з нафти або кам’яновугільної смоли, що утворюється в процесі коксування кам’яного вугілля. Так як потреба промисловості в аренах величезна, їх видобувають ще й способом каталітичної ароматизації вуглеводнів, що входять до складу нафти і мають ациклическое будова. В цьому випадку відбувається реакція дегидрогенизации – відщеплення атомів водню, в результаті чого, наприклад, з гексану можна одержати бензол. До хімії органічного синтезу продовжують застосовувати спосіб отримання бензолу з ацетилену. Реакція здійснюється при нагріванні этина до 600° і називається тримеризацией. Хімічні і фізичні властивості аренів хімія використовує в процесах отримання пластичних мас, лаків, барвників.

Бензол застосовують як добавки до палива. У сільському господарстві з’єднання – галогенопроизводные ароматичних вуглеводнів, служать інсектицидами – засобами для боротьби з комахами-шкідниками. Нітросполуки, наприклад, тринітротолуол, застосовують у військовій промисловості у якості вибухових речовин. Багато арени є добрими розчинниками.
У нашій статті ми вивчили хімічні та фізичні властивості аренів, і визначили області застосування цих сполук у промисловості.












