Хімічні властивості бензолу
З різноманітних хімічних властивостей аренів реакції заміщення слід згадати окремо. Також дуже значущі деякі реакції приєднання, які здійснюються в особливих умовах, і процеси окислення.
Реакції заміщення
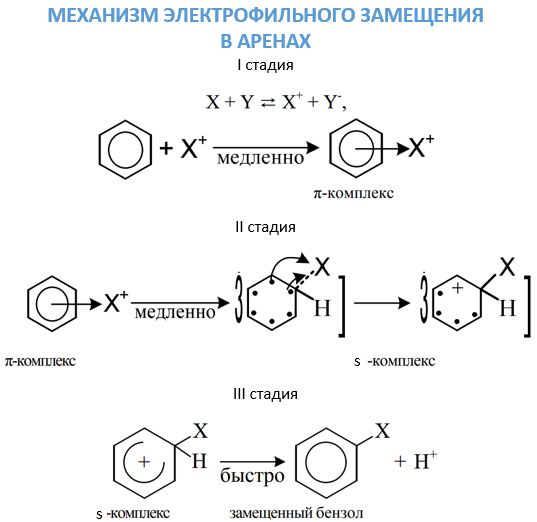
Досить рухливі π-електронами бензольного кільця, здатні дуже активно реагувати з атакуючими электрофилами. У такому электрофильном заміщення бере участь сама бензольное ядро в бензолі і пов’язана з ним вуглеводнева ланцюг у його гомологах. Механізм цього процесу досить детально вивчений органічною хімією. Хімічні властивості аренів, пов’язані з атакою електрофілов, виявляються за допомогою трьох стадій.
- Перша стадія. Поява π-комплексу через зв’язування π-електронної системи бензольного ядра з часткою Х+, яка зв’язується з шістьма π-електронами.
- Друга стадія. Перехід π-комплексу в s, обумовлений виділенням з шести π-електронів пари для утворення ковалентного зв’язку З—X. А інші чотири перерозподіляються між п’ятьма атомами З в бензольному кільці.
- Третя стадія. Супроводжується швидким відщепленням протона від s-комплексу.

Бромирование бензолу в присутності бромідів заліза або алюмінію без нагрівання призводить до отримання бромбензола:
C6Η6+ Br2 —> C6Η5-Br + ΗBr.
Нітрація сумішшю азотної і сірчаної кислот призводить до отримання сполук з нитрогруппой у кільці:
C6Η6+ ΗONO2 —> C6Η5—NO2+ Η2O.
Сульфування здійснюється бисульфониевым іоном, що утворюється в результаті реакції:
3Η2SO4 ⇄ SO3Η++ Η3O++ 2ΗSO4-,
або триоксид сірки.
Відповідає даному хімічному властивості аренів реакція:
C6H6+ SO3H+ —> C6H5—SO3H + H+.
Реакції алкильного і ацильного заміщення, або реакції Фріделя–Крафтса, проводять в присутності безводного AlCl3.
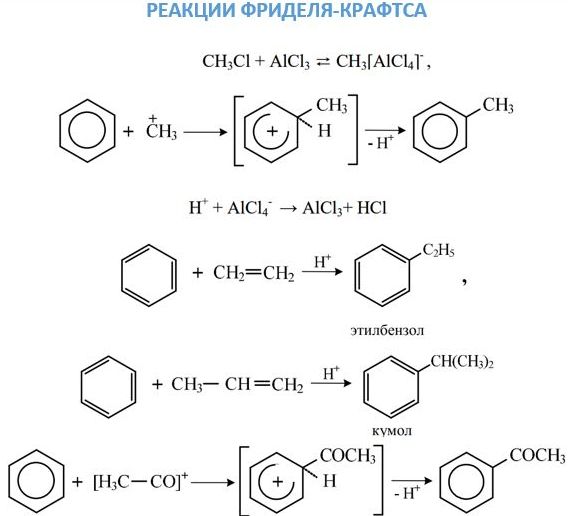
Ці реакції малоймовірні для бензолу і протікають з працею. Приєднання галогеноводнів та води до бензолу не відбувається. Однак при дуже високих температурах у присутності платини можлива реакція гідрування:
С6Н6 + 3Н2 —> С6Н12.
При опроміненні ультрафіолетом до молекулі бензолу можуть приєднатися молекули хлору:
С6Н6 + 3Cl2 —> C6Η6Cl6.