Чому реакції приєднання у аренів вимагають жорстких умов
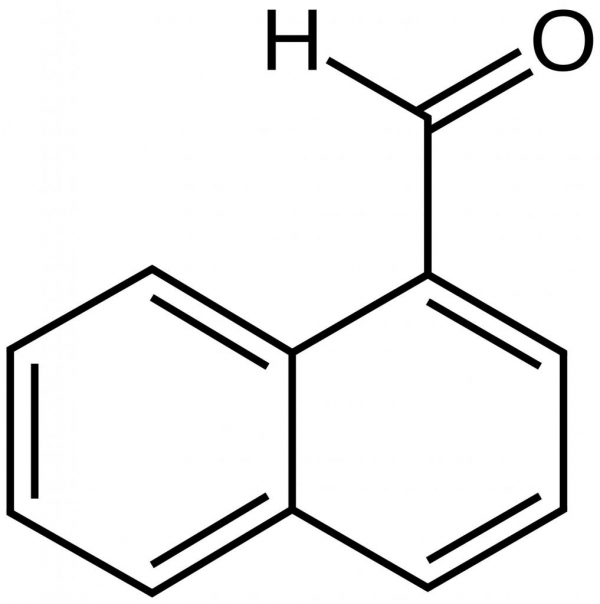
Головна особливість будови молекул ароматичних сполук полягає у наявності в їх молекулах бензольного кільця, що складається з шести перекриваються між собою p-електронів. Від нього залежать основні хімічні характеристики та фізичні властивості аренів. Для розриву полуторним зв’язку необхідна додаткова значна порція енергії. Її отримують, застосовуючи наступні параметри: ультрафіолетове випромінювання, високу температуру і тиск в реагуючої суміші, а також використовуючи каталізатори. Наприклад, хлор приєднується до бензолу тільки при опроміненні ультрафіолетовим світлом, утворюючи гексахлорциклогексану (гексахлоран). Він застосовується для протравлення деревини в процесі її тривалого зберігання, а також у сільському господарстві як засоби для боротьби з комахами-шкідниками.

C6H6 + 3Cl2 —світло—> C6H6Cl6 – приєднання
Алкилбензолы
Якщо атоми водню в молекулі бензолу замістити вуглеводневими радикалами, наприклад, метильным -CH3 або этильным -C2H5, то отримані ароматичні вуглеводні не є простою сумою властивостей алканів і аренів. Фізичні властивості та хімічні реакції, характерні для цих сполук, будуть мати ряд відмінностей. Так, толуол та етилбензол є безбарвними рідинами зі своєрідним запахом, легші за воду і нерозчинні в ній. Зате речовини добре розчиняються в органічних розчинниках, наприклад, ацетоні або дихлорметане. Їх самих також можна застосовувати як розчинник. У ароматичних вуглеводнів існують і специфічні характеристики. Поверхневий натяг, коефіцієнт дифузії, в’язкість – це фізичні властивості аренів, коротко описують їх характеристику, як органічних розчинників.