Фізичні властивості ацетилену
Ацетилен – це газ без кольору і запаху. Хоча домішки можуть давати йому часниковий запах. Практично не розчинний у воді, трохи розчинний в ацетоні. При температурі -83,8 °C зріджується.
Хімічні властивості ацетилену
Виходячи з потрійний зв’язку ацетилену, для нього будуть характерні реакції приєднання і реакції полімеризації. Атоми водню в молекулі ацетилену можуть заміщатися іншими атомами або групами. Тому можна сказати, що ацетилен проявляє кислотні властивості. Розберемо хімічні властивості ацетилену на конкретних реакціях.
Реакції приєднання:
- Гідрування. Здійснюється при високій температурі в присутності каталізатора (Ni, Pt, Pd). На палладиевом каталізаторі можливо неповне гідрування.
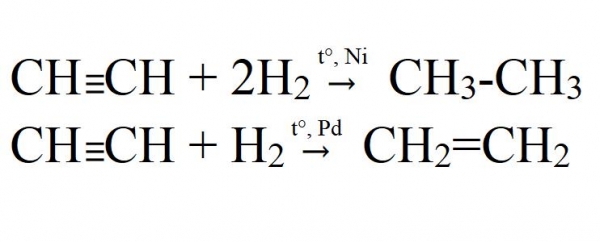
- Галогенирование. Може бути як частковим, так і повним. Йде легко навіть без каталізаторів або нагрівання. На світлі хлорування йде з вибухом. При цьому ацетилен повністю розпадається до вуглецю.
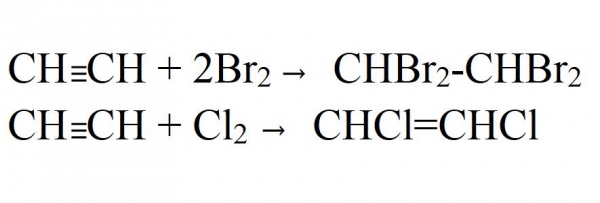
- Приєднання до оцтової кислоти і етилового спирту. Реакції йдуть тільки в присутності каталізаторів.
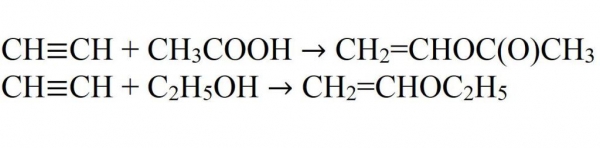
- Приєднання синильної кислоти.
CH≡CH + HCN → CH2=CH-CN
Реакції заміщення:
- Взаємодія ацетилену з метал-органічними сполуками.
CH≡CH + 2C2H5MgBr → 2C2H6 + BrMgC≡CMgBr
- Взаємодія з металевим натрієм. Необхідна температура 150 °C або попереднє розчинення натрію в аміаку.
2CH≡CH + 2Na → 2CH≡CNa + H2
- Взаємодія з комплексними солями міді і срібла.
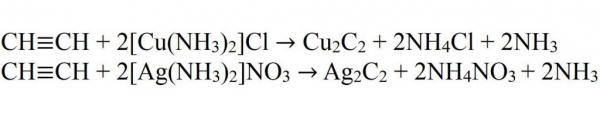
- Взаємодія з аміда натрію.
CH≡CH + 2NaNH2 → NaC≡CNa + 2NH3
Реакції полімеризації:
- Дімерізація. При цій реакції дві молекули ацетилену об’єднуються в одну. Необхідний каталізатор – сіль одновалентной міді.
- Трімерізація. У цій реакції три молекули ацетилену утворюють бензол. Необхідний нагрів до 70 °C, тиск і каталізатор.
- Тетрамеризация. В результаті реакції виходить восьмичленный цикл – циклооктатетраен. Для цієї реакції також потрібно невеликий нагрів, тиск і відповідний каталізатор. Зазвичай це комплексні сполуки двовалентного нікелю.

Це далеко не всі хімічні властивості ацетилену.